Выделяют травматическую и функциональную ИЦН.
Травматическая ИЦН. Во время различных внутриматочных вмешательств, связанных с предшествующим расширением шейки матки (аборты, диагностические выскабливания и др.) может повреждаться целостность мышечного кольца шейки. На месте повреждения формируется рубец, состоящий из соединительной ткани, не способный к сокращению и растяжению. Кроме того, формирование соединительной ткани на месте мышечной возможно после достаточно глубоких разрывов шейки матки во время предшествующих родов.
Функциональная ИЦН формируется на сроке 11–27 недель беременности, но чаще – в 16–25 недель. В этот период внутриутробного развития у плода начинают функционировать надпочечники, выделяющие среди прочих гормонов и андрогены – мужские половые гормоны. Если это дополнительное количество мужских половых гормонов «падает на почву» уже имеющегося у беременной женщины повышенного собственного уровня андрогенов, то под их действием шейка матки размягчается, укорачивается и раскрывается. При этом тонус матки может быть нормальным, и женщина, если она не посещает врача регулярно, может и не знать о формировании у неё ИЦН.
Влагалище заселено множеством бактерий. Это обстоятель¬ство имеет большое значение при уже сформировавшейся истмико-цервикальной недостаточности. Когда шейка матки укорачивается и приоткрывается, плодное яйцо инфицируется, плодные оболочки теряют свою прочность и происходит преждевременное излитие околоплодных вод.
Механизм самопроизвольного прерывания беременности при ИЦН состоит в том, что в связи с укорочением и размягчением шейки матки, зиянием внутреннего зева и канала шейки матки плодное яйцо лишается физиологической опоры в нижнем сегменте матки. При увеличении внутриматочного давления по мере развития беременности плодные оболочки выпячиваются в расширенный канал шейки матки, инфицируются и вскрываются, после чего происходит изгнание плодного яйца из полости матки (т.е. самопроизвольный выкидыш).
При отсутствии беременности органическую ИЦН можно диагностировать с помощью гистеросальпингографии (рентгеноконтрастного исследования матки), которое проводят во вторую фазу менструального цикла. При грубых анатомических изменениях шейки матки, обусловленных разрывами, необходимо оперативное лечение до беременности: выполнение пластики шейки матки. При наступлении беременности у женщин, перенесших пластическую операцию на шейке матки, родоразрешение проводят путем кесарева сечения. При функциональной или органической ИЦН, не требующей реконструктивной операции, подготовка к следующей беременности включает тщательное бактериологическое исследование содержимого канала шейки матки и антибактериальную терапию в течение 2—3 менструальных циклов в сочетании с физиотерапией. При гормональных нарушениях (гипофункция яичников, гиперандрогения) проводится соответствующая патогенетическая терапия.
Вовремя распознать ИЦН у беременной можно только при осмотре женщины на кресле. В нашей Клинике мы используем всё необходимое для своевременного выявления этого опасного состояния. Диагноз ИЦН во время беременности может быть установлен уже при осмотре шейки матки с помощью влагалищных зеркал и влагалищном исследовании. Врач может выявить сначала размягчение и укорочение шейки матки, а позже и зияние наружного зева шейки матки, и пролабирование плодного пузыря. В сомнительных случаях проводят специальное ультразвуковое исследование: влагалищным датчиком измеряют длину шейки матки и состояние внутреннего зева. Длина шейки матки менее 2 см и диаметр внутреннего зева более 1 см считаются ультразвуковыми признаками ИЦН.
Для лечения ИЦН у беременных могут быть использованы как оперативные, так и консервативные методы. Оперативное лечение включает в себя наложение кисетного шва на шейку матки. Операцию обычно проводят в период с 16-й по 18-ю недели беременности, в более поздние сроки беременности при выраженных клинических проявлениях ИЦН она менее эффективна.
К неоперативным методам лечения относят применение различных влагалищных пессариев (кольца Годжа, Мейера). Консервативные методы имеют ряд преимуществ: они бескровны, чрезвычайно просты и могут использоваться в амбулаторных условиях, но при выраженных проявлениях ИЦН они мало эффективны. Вместе с тем пессарии могут использоваться и после выполненной операции – для уменьшения давления на шейку матки и профилактики осложнений (свищей, разрывов шейки матки).
Симптомы ИЦН
К сожалению, признаки укорочения и расширения шейки матки практически невозможно идентифицировать: ощущения могут отсутствовать или ограничиваться тянущей или покалывающей болью внизу живота и / или поясницы. Но у кого из будущих мам их нет?
Недостаточность шейки матки может проявляться ощущениями покалывания и припухлости внизу живота, возвращающихся во влагалище, в прямую кишку. Если вы испытываете эти симптомы, вам следует обратиться к врачу.
Своевременная диагностика играет ключевую роль в выявлении заболевания. Что делать, если в ИЦН не было специфических симптомов и ничего не было сказано о состоянии здоровья?
Перед беременностью стоит оценить наличие описанных выше факторов риска. По возможности избегайте манипуляций с шейкой матки (и врачей, которые настаивают на травматическом лечении «эрозии»: в современной медицине диагнозы уже другие и оценка необходимости лечения в корне отличается от устаревшей). Хороший гинеколог при подготовке к зачатию – незаменимый врач при планировании пары!
Во время беременности консистенция шейки матки (при отсутствии рисков) оценивается в обычное время ультразвукового исследования – при обследованиях на 11-14 неделях, 16-17, 20-22, 30-32 неделях. Ультразвук измеряет состояние плода, плаценты, а также оценивает размер шейки матки, ее внутреннюю операционную систему и цервикальный канал.
Если есть повышенная вероятность ИЦН, или были преждевременные роды, или у них было двое или более детей одновременно, первое обследование проводится одновременно с первым обследованием – 11-14 недель, затем каждые две недели проводится назначенное УЗИ с оценкой длины шейки матки и ее консистенции.
Истмико-цервикальная недостаточность
ИЦН считают наиболее частой причиной прерывания беременности во втором триместре. Шейка матки при этой патологии не может удержать растущий плод: она укорачивается, плодный пузырь опускается вниз. Эти изменения приводят к угрозе или началу преждевременных родов, особенно при излитии околоплодных вод раньше срока.
Причины ИЦН бывают врождёнными и приобретёнными. Врождённые причины встречаются крайне редко. К приобретённым относят гормональные нарушения, инфекции половых путей и/или травмы шейки матки:
- искусственные аборты;
- стремительном течении предыдущих родов;
- рождении крупного плода (весом более 4 кг);
- грубых медицинских манипуляциях: выскабливании полости матки, биопсии эндометрия, удалении полипа цервикального канала.
Если будущая мать находится в группе высокого риска преждевременного рождения малыша, помимо заботы о здоровье и всех стандартных рекомендаций, необходимы и дополнительные мероприятия. Прежде всего, женщину постоянно должен наблюдать опытный врач, специализирующиеся на ведении беременности с осложнениями. В этом случае будущая мать может чаще посещать клинику, дополнительно проводить УЗИ, контролируя состояние шейки матки на протяжении беременности.
В зависимости от причин, которые приводят к преждевременным родам, могут потребоваться дополнительные методы лечения — прием гормональных препаратов, наложение швов на шейку матки, ношение пессария.
Ранее для того, чтобы ребенок не появился на свет раньше срока, рекомендовался постельный режим. По мнению экспертов, хотя постельный режим является своего рода «утешительным призом» при попытке предотвратить преждевременные роды, данные наблюдений за беременными показывают, что лежание не меняет сроков родов. А поскольку неподвижность не является полезной для мышц и суставов, не говоря уже о ее эмоциональных и психологических последствиях, длительный постельный режим имеет для матери реальные недостатки.
Поэтому сегодня тактика в отношении профилактики преждевременных родов изменилась. Врач будет максимально точно выяснять причину угрозы родов ранее срока и пытаться ее устранять вместе будущей матерью.
Все вышеизложенное подтверждает, что с беременностью, наступившей в результате применения программы ЭКО, необходимо относить к группе риска по развитию невынашивания беременности. Учитывая большое число факторов, определяющих статистически значимые различия в наступлении и течении гестации после применения программы ЭКО и естественного зачатия, а также трудности в определении непосредственного влияния каждого фактора, необходимо обеспечить персонализированный подход к курации женщин данной категории. При этом следует учитывать возраст женщины, ее соматический и акушерско-гинекологический анамнез, длительность бесплодия, особенности протоколов ВРТ и психоэмоциональное состояние во время беременности.
Несмотря на многочисленные масштабные исследования, посвященные выявлению факторов, неблагоприятно влияющих на течение одноплодной беременности, наступившей в результате применения программы ЭКО, так и не удается выяснить, чем же в большей мере определяется их отягощенное течение. Продолжаются споры о негативном влиянии самого факта бесплодия, а не способов оплодотворения. Нет единого мнения о весомости вклада особенностей протоколов ЭКО, факта бесплодия, психологического состояния женщины. Однако, опираясь на результаты собственных наблюдений и анализ клинических исследований, необходимо отметить, что, без сомнений, беременность, наступившую в результате применения программы ЭКО, следует рассматривать как гестацию с повышенным риском развития акушерских осложнений.
Начинать заботиться о здоровье малыша будущая мама может еще при планировании зачатия. Необходимым минимумом является отказ от вредных привычек, здоровый образ жизни, прием витаминных комплексов (фолиевой кислоты). Если в семейной истории бывали случаи преждевременных родов, об этом обязательно надо предупредить своего врача. После наступления беременности забота о здоровье будущей мамы не менее важна. Улучшение здоровья будущих мам поможет улучшить здоровье детей. Специальные программы ведения беременности (в том числе — после ЭКО) позволяют снизить риски преждевременного родоразрешения.
И в заключении, хотелось бы сказать, дорогие пациенты прислушивайтесь к рекомендациям своих врачей — репродуктологов, ведь «успешный» протокол — это не просто положительный тест на беременность, не двойня, рожденная на раннем сроке гестации, которая провела несколько месяцев в отделении детской реанимации; «успешный» протокол — это рожденный в срок здоровый малыш.
Привычное невынашивание беременности (привычный выкидыш)
Привычное невынашивание беременности, или привычный выкидыш, диагностируют в случае присутствия в анамнезе трех или более самопроизвольных выкидышей. Частота привычного невынашивания беременности не превышает 1% случаев. Риск самопроизвольного выкидыша (МВ) после 1 предварительного МВ равен 20-25%, после двух МВ — 25-30%, после трех — 30-35%.
Этиология привычного невынашивания беременности подобна таковой при самопроизвольных выкидышах:
- хромосомные аномалии,
- материнские системные болезни,
- анатомические дефекты матки,
- инфекции.
У 15% пациенток с привычным невынашиванием беременности обнаруживают антифосфолипидные антитела (антифосфолипидный синдром, АФС). У некоторых пациенток обнаруживают недостаточность лютеиновой фазы (НЛФ) менструального цикла, характеризующееся неадекватным уровнем прогестерона для поддержки беременности.
Диагностика. Пациентки с привычным выкидышем, а также при наличии в анамнезе двух самопроизвольных абортов подлежат обследованию по выявлению этиологического фактора этого осложнения. Алгоритм обследования этих пациенток состоит из следующих мероприятий:
1) исследование кариотипа родителей и кариотипов всех продуктов оплодотворения;
2) оценка анатомического строения половых органов матери (ультрасонография, гистеросальпингография (ГСГ));
3) эксплоративная гистероскопия и / или лапароскопия при аномальных или неопределенных результатах ГСГ;
4) проведение скрининговых тестов на гипотиреоидизм, сахарный диабет, АФС, коагулопатии, системная красная волчанка. Эти тесты включают анализ на волчаночный антикоагулянт (дополнительно — антикардиолипиновые антитела, протеин 8 и протеин С, дефицит фактора V, антиядерные антитела (АЯА);
5) определение сывороточного уровня прогестерона в лютеиновую фазу менструального цикла и измерения базальной температуры (снижение уровня прогестерона <10 нг / мл через 7 дней после овуляции свидетельствует о недостаточности лютеиновой фазы цикла, сокращение продолжительности лютеиновой фазы <11 дней);
6) исследование содержимого влагалища, шейки матки и эндометрия для исключения возможной инфекции;
7) биопсия эндометрия в лютеиновую фазу для определения соответствия его структуры дню менструального цикла, наличии децидуальной или пролиферативных изменений.
Диагноз недостаточности лютеиновой фазы цикла определяют, если при двух пробах эндометрия через 7 дней после овуляции задержка гистологических изменений превышает 2 дня.
Лечение больных с привычным выкидышем зависит от его этиологии и должно быть индивидуализированным. В 30-50% случаев причинный фактор выявить не удается. Пациенткам с хромосомными аномалиями, в частности сбалансированными транслокациями, предлагаются вспомогательные репродуктивные технологии (фертилизация с применением донорских сперматозоидов или яйцеклеток).
Анатомические аномалии по возможности корректируют хирургическим путем. При истмико-цервикальной недостаточности накладывают шов (серкляж) на шейку матки. Пациенткам с недостаточностью лютеиновой фазы цикла назначают лечение прогестинами (дюфастон, утрожестан, 17-оксипрогестерона капронат). При наличии АФС применяют низкие дозы аспирина (75-80 мг / сут) или гепарин.
Интересные факты
В середине 90-х годов прошлого века Шведский национальный совет по здравоохранению и социальному обеспечению инициировал создание национального реестра по ЭКО, включающего всех детей, рожденных с помощью ВРТ, начиная с 1982 г. Первое реестровое исследование, в котором сравнивались акушерские исходы рождаемости детей, зачатых с помощью ЭКО и естественным путем, было опубликовано в Ланцете в 1999г.
В исследовании проанализированы акушерские исходы рождаемости первой группы шведских детей, зачатых с помощью ЭКО, и продемонстрированы в 5–6 раз более высокие риски преждевременных родов, рождения детей с низкой и очень низкой массой тела, после применения ВРТ по сравнению с детьми из общей популяции. Перинатальная смертность составила 1,9 и 1,1% у детей, рожденных с помощью ВРТ, и детей из общей популяции соответственно. Частота многоплодных родов у матерей при использовании ВРТ составила 26%. Несмотря на снижение частоты многоплодных родов в последние годы, ее показатели все еще остаются высокими в большинстве стран. Последние отчеты демонстрируют, что частота многоплодных родов в Европе составила 15% в 2019 г., в США — 24% в 2018 г. Из них 95% приходились на роды двойней. Хорошо известно, что материнская и неонатальная заболеваемость и смертность у пациенток, прибегших к зачатию с помощью ВРТ, значительно выше при беременностях двойней, нежели при одноплодных беременностях.
Лучший способ свести к минимуму риск многоплодных родов — уменьшить число переносимых эмбрионов. Первое исследование, демонстрирующее селективный перенос одного эмбриона как успешный для программ ЭКО, было представлено в Финляндии. Страны Скандинавии, в частности Швеция, являются ведущими в снижении частоты многоплодных родов путем внедрения селективного переноса как основной стратегии лечения. Как следствие, частота многоплодных родов снизилась с 26% в 2001 г. до 5–6% в 2010 г., тогда как частота родов в общем не изменилась. Частота селективных переносов возросла с 10% в 2000 г. до 70–80% от всех переносов в свежих циклах и стабилизировалась в последние годы. Для криоциклов частота селективных переносов на настоящий момент составляет 85%.
Почему начинается шеечная недостаточность и чем она грозит
Недостаточность шейки матки определяется у 7-9% беременных женщин во II триместре беременности. Это состояние в гинекологии называют истомико-цервикальной недостаточностью (ИЦН) и считают серьезной угрозой выкидыша и преждевременных родов.
Шейка матки состоит из мышечной и соединительной ткани. Мышцы, сконцентрированные в верхней части, образуют плотное кольцо (сфинктер). В норме оно легко выдерживает нагрузку во время беременности и не дает матке открыться до родов.
Если мышечные волокна ослабляются, возникает шеечная недостаточность: шейка укорачивается, сфинктер расслабляется. Плодный пузырь проскакивает в получившееся отверстие — в зависимости от срока беременности диагностируют выкидыш или преждевременные роды.
Через приоткрытый цервикальный канал в матку легко проникают микробы, вызывающие инфицирование плодных оболочек и послеродовые гнойные осложнения.
Недостаточность бывает первичной и вторичной.
Результаты
Из 71 первородящей женщины в анамнезе у 31(43,66 %) были воспалительные заболевания женских половых органов, у 4 (5,63 %) — эрозия шейки матки, у 20 (28,17 %) — экстрагенитальная патология (сердечно-сосудистые заболевания), у 16 (22,54 %) пациенток — эндокринная патология (ожирение), женщин с благоприятным анамнезом не было (рис. 1).
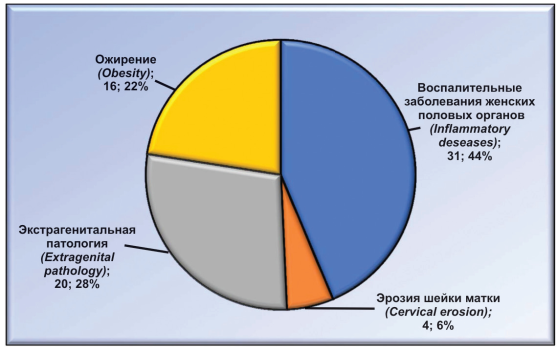
Рисунок 1. Распределение анамнестических данных у первородящих женщин.
Figure 1. Distribution of anamnestic data among primiparous women.
Из 87 повторнородящих женщин в анамнезе у 33 (37,93 %) был воспалительный процесс женских половых органов, у 9 (10,34 %) — эрозия шейки матки, у 18 (20,69 %) — экстрагенитальная патология (сердечно-сосудистые заболевания), у 20 (22,99 %) — эндокринная патология (ожирение), у 7 (8,05 %) женщин анамнез был благоприятный (рис. 2).
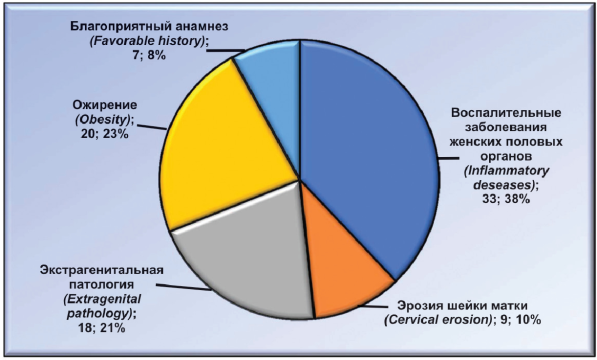
Рисунок 2. Распределение анамнестических данных у повторнородящих женщин.
Figure 2. Distribution of anamnestic data among multiparous women.
Беременность в первой группе у 12(16,90 %) из 71 женщины осложнилась анемией, у 9 (12,68 %) — гестационным пиелонефритом, у 15 (21,13 %) — фето-плацентарной недостаточностью (ФПН). Из 87 повторнородящих второй группы беременность осложнилась у 19 (21,84 %) анемией, у 13 (14,94 %) — ФПН, у 8 (9,20 %) — обострением хронического пиелонефрита. Диагноз истмико-цервикальной недостаточности ставился на основании совокупности данных гинекологического обследования и трансвагинального ультразвукового исследования шейки матки. Скрининг трансвагинального ультразвукового исследования шейки матки проводился на 13 — 14-й, 18 — 21-й, 30 — 31-й неделях беременности (согласно приказу № 572н МЗ России). Скрининг трансвагинального ультразвукового исследования выявил интересную картину. Так, у первородящих женщин первой клинической группы ИЦН была диагностирована у 32 (45,07 %) пациенток на 13 — 14-й неделе беременности, у 29 (40,85 %) — на 17 — 18-й неделе, у 10 (14,08 %) — на 33 — 34-й неделе. У повторнородящих второй клинической группы из 87 женщин ИЦН у 39 (44,83 %) была диагностирована на 13 — 14-й неделе беременности, у 34 (39,08 %) — на 18 — 21-й неделе, у 14 (16,09 %) — на 30 — 32-й неделе (рис. 3).
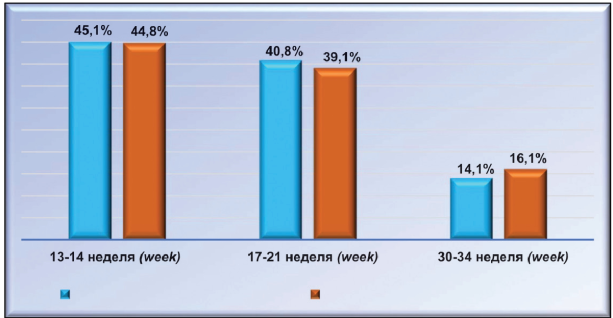
Рисунок 3. Время выявления ИЦН у первородящих и повторнородящих.
Figure 3. Time of identify ICN amongprimiparous and multiparous women.
Интересен тот факт, что морфологические изменения шейки матки, характерные для ИЦН не всегда сопровождались клиническими признаками угрожающего прерывания беременности. Так, из 71 женщины первой клинической группы у 29 (40,85 %) жалобы на ноющие боли внизу живота отсутствовали. У 42 (59,15 %) ИЦН сопровождалась болевым синдромом, причем у 18 (42,86 %) он появлялся на 13 — 14-й неделе беременности, у 15 (35,71%) — на 18 — 21-й неделе, у 9 (21,43%) — на 30 — 32-й неделе. Из 87 повторнородящих второй клинической группы у 41(47,13 %) женщины при наличии ИЦН болевой синдром отсутствовал, а у 46 (52,87 %) он имел место. Болевой синдром появлялся у 25 (54,35 %) на 13 — 14-й неделе, у 13 (28,26 %) — на 18 — 21-й неделе, y 8 (17,39 %) — на 30 — 32-й неделе беременности (рис. 4).
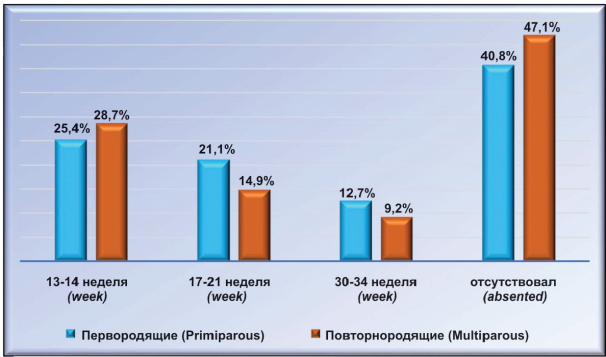
Рисунок 4. Сроки появления болевого синдрома при ИЦН у перво- и повторнородящих.
Figure 4. The timing of the onset of pain with ICI among primiparous and multiparous women.
Из 71 женщины первой клинической группы самостоятельно родили через естественные родовые пути 64 (90,14 %) беременных, у 7(9,86 %) было абдоминальное родоразрешение (рис. 5.)

Рисунок 5. Исход родов у первородящих женщин.
Figure 5. Birth outcome among primiparous women.
Показанием к операции были тазовое предлежание плода, анатомический и клинически узкий таз. В срок родили из 71 беременной 46 (64,79 %), у 19 (26,76 %) роды произошли на 35 — 36-й неделе беременности, у 6 (8,45 %) женщин — после 41-й недели.
Из 87 женщин второй клинической группы 79 (90,80 %) родили через естественные родовые пути, 8 (9,20 %) — путем операции кесарево сечение (рис. 6).
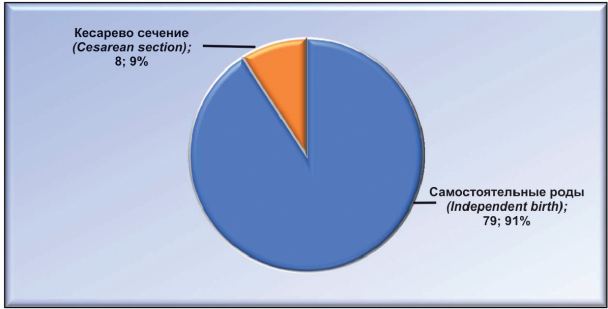
Рисунок 6. Исход родов у повторнородящих женщин.
Figure 6. The outcome of childbirth among multiparous women.
Показанием к операции были неправильное положение плода, миопия высокой степени, клинически узкий таз. В срок родили 69 (79,31 %) женщин, 11 (12,64 %) — на 35 — 36-й неделе, 7 (8,05 %) — после 41-й недели. Вес родивших детей у первородящих колебался от 2700 до 3900, у повторнородящих, соответственно, от 3400 до 4100.
Консервативное лечение ИЦН
Протокол лечения предполагает применение консервативных методик в легких случаях ИЦН, а также при ее гормональной природе. Проведение коррекции гормональных нарушений при помощи необходимых препаратов помогает восстановить уровень гормонов и прекратить дальнейшее размягчение шейки. При дефиците прогестерона назначаются Утрожестан или Дюфастон — синтетические аналоги прогестерона на курс 1-3 месяца и более. Достоинство препаратов — в быстром прекращении размягчения шейки матки и остановке прогрессирования ИЦН. Гиперандрогению лечат путем приема глюкокортикостероидов (Преднизолон, Дексаметазон) короткими курсами (до 14-20 дней), ведь эти препараты снижают иммунитет и могут нанести вред ребенку.
Еще один эффективный неоперативный метод – наложение кольца Мейера (пессария) для сужения шейки. Это резиновое кольцо, которое краями упирается во влагалище и удерживает зев матки в закрытом состоянии. Срок установки кольца может быть любым. Применяется метод и при необходимости оттянуть роды.
Кольцо Мейера нужно регулярно промывать для дезинфекции. Обязательно периодически брать мазки из влагалища во избежание инфицирования. Обычно снимают кольцо после 38 недель.
Патогенез и этиология ИЦН
Патогенетическими факторами ИЦН могут быть функциональные или структурные дефекты шейки матки, соответственно ИЦН подразделяются на функциональную и анатомическую (органическую) формы. Функциональный ИЦН является результатом эндокринных нарушений и определяется стимуляцией α-рецепторов и ингибированием β-адренорецепторов. При гиперэстрогении повышается чувствительность и активация α-рецепторов, что приводит к сокращению шейки матки и расширению цервикального канала. В результате с увеличением концентрации прогестерона повышается чувствительность рецепторов и отсутствуют структурные изменения шейки матки в сторону образования ИЦН. В 30% случаев функциональный ИКМ сопровождается гиперандрогенизмом. И, наконец, функциональный ИЦН может образоваться в результате нарушения взаимоотношений между мышечными волокнами и соединительной тканью в шейке матки с преобладанием первых, что приводит к раннему размягчению шейки матки.
Анатомическая (органическая) ИЦН является результатом посттравматических изменений структуры шейки матки: механического расширения цервикального канала перед выскабливанием матки, разрывов шейки матки при родах, особенно не восстановившихся, образующих рубцовую деформацию шейки матки.
Пациенты с ИЦН также характеризуются наличием повторных внутриматочных вмешательств, ЧР, в анамнезе поздним прерыванием беременности, хирургическим лечением шейки матки, а ранняя беременность при ИЦН гораздо чаще характеризуется клинической угрозой прерывания беременности и / или или PR.
В современной литературе ключевым звеном в патогенезе ИЦН является дисплазия соединительной ткани из-за нарушения синтеза коллагена. Шейка матки – фиброзный орган, и во время беременности она претерпевает структурные изменения, связанные с ее созреванием (преждевременным или своевременным), что определяет начало родов. При дисплазии соединительной ткани (CTD), особенно в ее недифференцированных формах (UDCT), происходит преждевременное созревание шейки матки и формируется ИЦН. Дефицит магния занимает видное место в патогенезе летнего времени. При дефиците магния фибробласты теряют способность вырабатывать коллаген. Ионы магния входят в состав соединительной ткани и участвуют в регуляции ее метаболизма, являясь кофактором ремоделирования соединительной ткани. Это обстоятельство может быть связано с включением препаратов магния в схему профилактИЦН и лечения угрозы прерывания беременности
Способы лечения ИЦН
С целью профилактики преждевременных родов при истмико-цервикальной недостаточности с 20 по 34 недели беременности назначаются препараты прогестерона (ДЮФАСТОН, УТРОЖЕСТАН) – гормона, вырабатывающегося в плаценте и поддерживающего беременность.
Существуют два способа лечения истмико-цервикальной недостаточности. Это нехирургические методы и хирургические.
Нехирургические методы
К нехирургическим методам относят введение во влагалище специальных акушерских пессариев – колец, которые надеваются на шейку матки и препятствуют ее дальнейшему раскрытию, поддерживая предлежащую часть плода. Нехирургические методы имеют ряд преимуществ – они не требую госпитализации в стационар, введения наркоза и просты в использовании. Применяют пессарии обычно после 28 недель беременности. Перед введением кольца обязательно берут мазок на флору для выявления и лечения возможного воспалительного процесса. После введения акушерского пессария необходимо каждые 2-3 недели проводить обработку влагалища и кольца антисептическими растворами для профилактики развития инфекции. Однако не всегда этот метод может быть применим.
Хирургические методы
При выраженной истмико-цервикальной недостаточности применение колец неэффективно. Не используют их также при выбухании плодного пузыря в канал шейки матки. В этих случаях лечение осуществляется путем зашивания шейки матки.
Показания к хирургической коррекции ИЦН:
- наличие ранее самопроизвольных выкидышей и преждевременных родов во 2-3 триместрах
- прогрессирующая по данным клинического обследования недостаточность шейки матки, длина шейки матки менее 25 мм по данным трансвагинального УЗИ.
Противопоказания к хирургическому лечению:
- повышенная возбудимость матки, тонус
- заболевания, являющиеся противопоказанием для сохранения беременности, например тяжелые заболевания печени, сердечно-сосудистой системы, инфекционные, генетические заболевания,
- кровотечение,
- пороки развития плода,
- наличие патогенной флоры во влагалище, воспаление влагалища.
Наложение швов на шейку матки обычно проводится с 13 до 27 недели беременности. Сроки проведения операции определяются индивидуально лечащим врачом. Наиболее благоприятны для оперативного лечения срок с 15 по 19 неделю беременности, когда открытие шейки матки не очень выражено и плодный пузырь не выбухает в канал.
Наложение швов на шейку матки производят под общим наркозом. В ряде случаев, например при выбухании нижнего полюса плодного яйца в канал шейки матки, после операции, в целях профилактики возможного инфицирования плодных оболочек, назначаются курс антибиотиков. При неосложненном течении послеоперационного периода беременная выписывается домой через 5-7 дней после операции. Однако каждые 2 недели врач женской консультации должен осматривать шейку матки и брать мазки на флору.
Самым частым осложнением после хирургической коррекции истмико-цервикальной недостаточности является прорезывание тканей шейки матки нитью. Это может наступить, если шейка поражена воспалительным процессом или если начинаются сокращения матки, то есть родовая деятельность. Чтобы избежать сокращений матки после наложения швов многим пациенткам назначаются токолитики – препараты снимающие тонус матки.
Швы с шейки матки снимают в 37 – 38 недель беременности. Это производят при осмотре шейки матки в гинекологическом кресле. Процедура снятия швов обычно совершенно безболезненна.
Диагностика
Пациентки могут жаловаться на влагалищные выделения, кровотечение или истечение околоплодных вод (разрыв оболочек). Иногда беременную могут беспокоить несильные сокращения матки или ощущение давления в животе или влагалище. При обследовании шейки матки в зеркалах, при вагинальном и ультразвуковом исследовании обнаруживают раскрытия шейки матки и выпячивание плодного пузыря через шеечный канал во влагалище.
Структурные изменения шейки матки более выражены, чем ожидаемы. В этих обстоятельствах могут возникать трудности при дифференциальной диагностике с преждевременными родами, но отсутствие выраженных болевых ощущений при прогрессирующем расширении шейки матки свидетельствует о наличии ИЦН.
Лечение должно быть индивидуализированным. При нежизнеспособном плоде (срок беременности до 24 нед) накладывают стягивательный шов на шейку матки (серкляж) или, реже, выбирают выжидательную тактику. В случае необходимости беременность завершают. При жизнеспособном плоде назначают строгий постельный режим, кортикостероиды (дексаметазон, бетаметазон) для ускорения созревания легких плода. При наличии маточных сокращений выполняют токолиз.
Лечение истмико-цервикальной недостаточности
Серкляж — шов, который накладывается вагинальным доступом вокруг шейки матки на уровне шеечно-влагалищного соединения (серкляж Макдональда) или внутреннего зева (серкляж Широдкара). Целью этого шва является закрытие шейки матки. Существуют многочисленные модификации стяжные шва на шейку матки при ИЦН (циркулярный, П-образный шов и т.д.).
Серкляж выполняется в сроке 12-14 нед гестации. При этой операции бывают такие осложнения:
- разрыв плодных оболочек,
- преждевременные роды,
- инфекция.
Пациенткам с ИЦН, в которых 1-2 попытки вагинального серкляж на шейку матки были неэффективными, предлагают трансабдоминальный серкляж в сроке 12-14 нед или перед ожидаемой беременностью. Шов с шейки матки снимают в сроке 36-38 нед гестации. Родоразрешение пациенток, которым выполнялся трансабдоминальный серкляж на шейку матки, проводится путем кесарева сечения.


































